Standardbildungsenthalpie ∆Hf0
allgemein: Enthalpie ist der Wärmeinhalt eines Systems (bei konstantem Druck)
Def.: Elemente in ihrem stabilsten Zustand besitzen bei 101kPa Druck und 298 K absoluter Temperatur (Standardbedingungen) die Enthalpie = 0
Def.: Die molare Standardbildungs-Enthalpie stellt die Wärme dar, die bei der Bildung einer Verbindung aus Elementen im Standardzustand mit der Umgebung ausgetauscht wird.
Standardeaktionsenthalpie ∆HR0
Formel für die Ermittlung der Standardreaktionsenthalpie:
∆HR0 = ∑∆Hf0(Produkte)
- ∑∆Hf0(Edukte)
Entropie S
Die Entropie ist der Quotient aus Wärmemenge in Joule und Temperatur in Kelvin
S = Q / T
Einheit: [Joule/K]
Es wird nun ein System aus einem warmen und einem kalten Körper betrachtet.
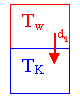
Für den kälteren bzw. wärmeren Körper sind die Änderung der Entropien wie folgt definiert:
dSK = dq / TK
dSw = dq / Tw
Die Entropieänderung des Gesamtsystems erhält man durch folgende Gleichung:
dS = dq / Tk - dq / Tw
> 0 (da Tw > Tk
Bei einem spontan (freiwillig) ablaufenden Vorgang ist die Entropieänderung dS > 0. Erreicht die Temperatur des warmen Körpers die des kalten Körpers kommt der Vorgang zum erliegen.
Für Entropien ist eine Absolutwertangabe möglich, die sogennante
molare Standardentropie S0
Einheit: [J/(mol x K)]
Reaktionsentropie
Die Reaktionsentropie wird mit folgender Gleichung ermittelt:
∆SR0 = ∑∆S0(Produkte)
- ∑∆S0(Edukte)
Freie Enthalpie
Mit nachfolgender Formel kann die freie Enthalpie bestimmt werden:
∆GR = ∆HR0
- ( T x ∆SR0
)
Mit Hilfe der freien Entropie können über eine Reaktion folgende Aussagen getroffen werden:
- freie Entalpie > 0 ; chem. Reaktion findet nicht (freiwillig) statt
- freie Entalpie < 0 ; chem. Reaktion kann stattfinden
- freie Entalpie = 0 ; chem. Reaktion hat bereits stattgefunden bzw. ist im Gleichgewicht

